
O que previne:
Tuberculose – principalmente as formas graves, como meningite tuberculosa e tuberculose miliar (espalhada pelo corpo).
Do que é feita:
É composta pelo bacilo de Calmette-Guérin – origem do nome BCG – obtido pela atenuação (enfraquecimento) de uma das bactérias que causam a tuberculose. Completam sua composição o glutamato de sódio e a solução fisiológica (soro a 0,9%).
Indicação:
A vacina é indicada de rotina a partir do nascimento até antes de a criança completar 5 anos de idade.
Pessoas de qualquer idade que convivem com portadores de hanseníase (lepra).
Contraindicação:
Esquema de doses:
Dose única.
Local de aplicação:
Intradérmica.
Cuidados antes, durante e após a vacinação:
A vacinação não requer qualquer cuidado prévio.
Na maioria das vezes, haverá uma reação no local da aplicação com posterior formação de cicatriz. É importante não colocar produtos, medicamentos ou curativos, pois trata-se de uma resposta esperada e normal à vacina.
A revacinação de crianças que não desenvolveram cicatriz deixou de ser recomendada pelo Ministério da Saúde em fevereiro de 2019.
Efeitos e eventos adversos:
A BCG quase sempre deixa uma cicatriz característica, com até 1 cm de diâmetro, no local em que foi aplicada – como rotina, no braço direito. Essa reação é esperada! A resposta à vacina demora cerca de três meses (12 semanas), podendo se prolongar por até seis meses (24 semanas), e começa com uma mancha vermelha elevada no local da aplicação, evolui para pequena úlcera, que produz secreção até que vai cicatrizando.
Eventos adversos possíveis: úlceras com mais de 1 cm ou que demoram muito a cicatrizar; gânglios ou abscessos na pele e nas axilas; disseminação do bacilo da vacina pelo corpo, causando lesões em diferentes órgãos.
Segundo o Ministério da Saúde (MS), os gânglios surgem em cerca de 10% dos vacinados.
Qualquer que seja o evento, o serviço de vacinação deve notificá-lo ao órgão de vigilância em Saúde e encaminhar o paciente ao posto de saúde para acompanhamento e tratamento adequados.
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne
Infecção causada pelos quatro sorotipos de dengue : DEN1, DEN2, DEN3 e DEN4. A eficácia na prevenção da doença é de 65,5%; na prevenção de dengue grave e hemorrágica é de 93% e de internação é de mais de 80%.
Do que é feita
Trata-se de vacina atenuada, composta pelos quatro sorotipos vivos do vírus dengue, obtidos separadamente por tecnologia de DNA recombinante. Contém ainda aminoácidos essenciais (incluindo fenilalanina), aminoácidos não essenciais, cloridrato de arginina, sacarose, trealose di-hidratada, sorbitol, trometamol e ureia. O diluente é constituído por cloreto de sódio e água para injeções. Não contém adjuvantes e conservantes.
Indicação
A vacina está licenciada para crianças a partir de 9 anos de idade, adolescentes e adultos até 45 anos e é recomendada para indivíduos previamente infectados por um dos vírus da dengue (soropositivos com ou sem história da doença).
Contraindicação
Esquema de doses
Três doses com intervalo de seis meses.
Local de aplicação
Subcutânea.
Cuidados antes, durante e após a vacinação
É sugerido avaliar com seu médico a indicação da vacina, já que em pessoas vacinadas não infectadas previamente foi observado um risco aumentado de hospitalização e dengue com sinal de alarme (saiba mais em efeitos e eventos aversos).
Adiar a vacinação em caso de doença febril aguda moderada a grave.
A vacinação de pessoas portadoras do vírus HIV deve ser avaliada por médico, que pode prescrevê-la se não houver comprometimento do sistema imunológico.
Em pacientes que receberam tratamento com doses elevadas de corticosteroides sistêmicos por duas semanas ou mais, é preciso adiar a vacinação até a função imunológica estar restaurada (no mínimo quatro semanas após a interrupção do tratamento).
As mulheres em idade fértil devem evitar engravidar por quatro semanas após vacinação.
Preferencialmente, não aplicar no mesmo momento em que outras vacinas são administradas.
Efeitos e eventos adversos
As reações adversas mais frequentemente relatadas foram: dor de cabeça, dor no local da injeção, mal-estar e mialgia.
As reações foram geralmente de gravidade leve a moderada e de curta duração (até três dias). O início foi tipicamente observado em até três dias após a vacinação, com exceção da febre, que surge dentro de 14 dias após a aplicação da vacina.
As reações adversas sistêmicas tendem a ser menos frequentes após a segunda e a terceira doses.
Reações adversas possíveis:
OBS: a febre foi menos frequente nos indivíduos com mais de 18 anos de idade. Hematoma e coceira no local da injeção foram menos frequente indivíduos dos 9 aos 17 anos de idade.
OBS: A vacina não causa a doença.
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
Contém toxoides diftérico e tetânico, derivados das toxinas produzidas pelas bactérias causadoras das doenças; tem o sal de alumínio como adjuvante, cloreto de sódio, e água para injeção.
Indicações:
A vacina é utilizada na rede pública para a proteção das pessoas que não iniciaram ou não terminaram o esquema contra difteria e tétano até os 7 anos de idade e para as doses de reforço a cada dez anos.
Contraindicações:
Apenas pessoas com alergia grave (anafilaxia) a algum dos componentes da vacina ou a dose anterior.
Esquema de doses:
Sempre que possível, a dT deve ser substituída pela tríplice bacteriana acelular do tipo adulto (dTpa), que também previne a coqueluche.
Para crianças a partir de 7 anos de idade, adolescentes e adultos com:
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Sintomas de eventos adversos persistentes, que se prolongam por mais de 24-72 horas, devem ser investigados para verificação de outras causas.
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
Contém toxoides diftérico e tetânico, derivados das toxinas produzidas pelas bactérias causadoras das doenças, sal de alumínio como adjuvante, cloreto de sódio, e água para injeção.
Indicação:
Para crianças menores de 7 anos de idade, que tenham apresentado encefalite nos sete dias subsequentes à administração de dose anterior de vacina contendo componente coqueluche (DTPw ou DTPa).
Contraindicações:
Esquema de doses:
Uma a três doses, de acordo com o histórico de cada criança e sob orientação médica.
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Difteria , tétano e coqueluche .
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
Contém os toxoides diftérico e tetânico (derivados das toxinas produzidas pelas bactérias causadoras das doenças), e componentes da cápsula da bactéria da coqueluche (Bordetella pertussis), sal de alumínio como adjuvante, fenoxietanol, cloreto de sódio e água para injeção.
A quantidade de toxoide diftérico e de componentes pertussis é menor que na vacina infantil (DTPa).
Indicações:
Contraindicação:
Pessoas que apresentaram anafilaxia ou sintomas neurológicos causados por algum componente da vacina ou após a administração de dose anterior.
Esquema de doses:
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Difteria , tétano e coqueluche .
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
Contém os toxoides diftérico e tetânico (derivados das toxinas produzidas pelas bactérias causadoras das doenças), e componentes da cápsula da bactéria da coqueluche (Bordetella pertussis), sal de alumínio como adjuvante, fenoxietanol, cloreto de sódio, e água para injeção.
Indicações:
Crianças com menos de 7 anos de idade. Mesmo as que já tiveram tétano, difteria, doença causada pelo Haemophilus influenzae tipo b (Hib) e/ou coqueluche devem ser imunizadas, uma vez que estas doenças não conferem proteção permanente frente a novas infecções.
Contraindicações:
Esquema de doses:
Para a vacinação rotineira de crianças (aos 2, 4, 6 meses e entre 12 e 18 meses), preferir a vacina quíntupla (penta) ou hexa, nas quais a DTPa é combinada a outras vacinas. Ver DTPa-VIP/Hib ou DTPa-VIP-HB/Hib . Para a dose de reforço entre 4 e 5 anos de idade, a DTPa pode ser substituída por dTpa ou dTpa-VIP .
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Com a vacina DTPa os eventos adversos são menos frequentes e intensos do que com a DTPw.
Manifestações locais:
Manifestações sistêmicas:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Difteria , tétano , coqueluche e poliomielite .
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
Contém os toxoides diftérico e tetânico (derivados das toxinas produzidas pelas bactérias causadoras das doenças), componentes da cápsula da bactéria da coqueluche (Bordetella pertussis), vírus da poliomielite inativados (mortos) tipos 1, 2 e 3, sal de alumínio como adjuvante, 2-fenoxietanol, polissorbato 80, cloreto de sódio e água para injeção.
Pode conter ainda traços de formaldeído, neomicina e polimixina B usados no processo de fabricação.
Indicações:
Contraindicação:
Pessoas que apresentaram anafilaxia após uso de componentes da vacina ou dose anterior.
Esquema de doses:
Pode substituir qualquer dose de dTpa . Em caso de viagens a locais de risco para a poliomielite, pode ser aplicada mesmo em pessoas que estejam em dia com a dTpa.
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Difteria , tétano e coqueluche .
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
Contém os toxoides diftérico e tetânico (derivados das toxinas produzidas pelas bactérias causadoras das doenças); bactéria morta da coqueluche (Bordetella pertussis); sal de alumínio como adjuvante, cloreto de sódio, e água para injeção.
Indicações:
Para todas as crianças até 7 anos de idade, mesmo as que já tiveram tétano, difteria e coqueluche, uma vez que estas doenças não conferem proteção permanente. A vacina é usada na rede pública como dose de reforço para crianças com idade entre 4 e 5 anos.
Contraindicações:
Esquema de doses:
É utilizada na rotina pública de vacinação infantil aos 2, 4 e 6 meses de idade, na apresentação combinada com as vacinas Hib e hepatite B. A vacina DTPw isolada (não combinada a outras vacinas) é usada na rede pública para os reforços do segundo ano de vida e dos 4 anos de idade.
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Manifestações locais: vermelhidão, calor, endurecimento, dor e inchaço no local da aplicação ocorrem em 37% a 50% dos casos e podem atrapalhar a movimentação do membro. Ocasionalmente pode aparecer nódulo endurecido, indolor e que desaparece ao longo de várias semanas. Com menos frequência, pode haver formação de abscesso no local da aplicação, em geral estéril (sem infecção associada: abscesso frio) ou infectado com pus (abscesso quente).
Manifestações sistêmicas: relacionam-se sobretudo com o componente pertussis (coqueluche) da vacina e incluem:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
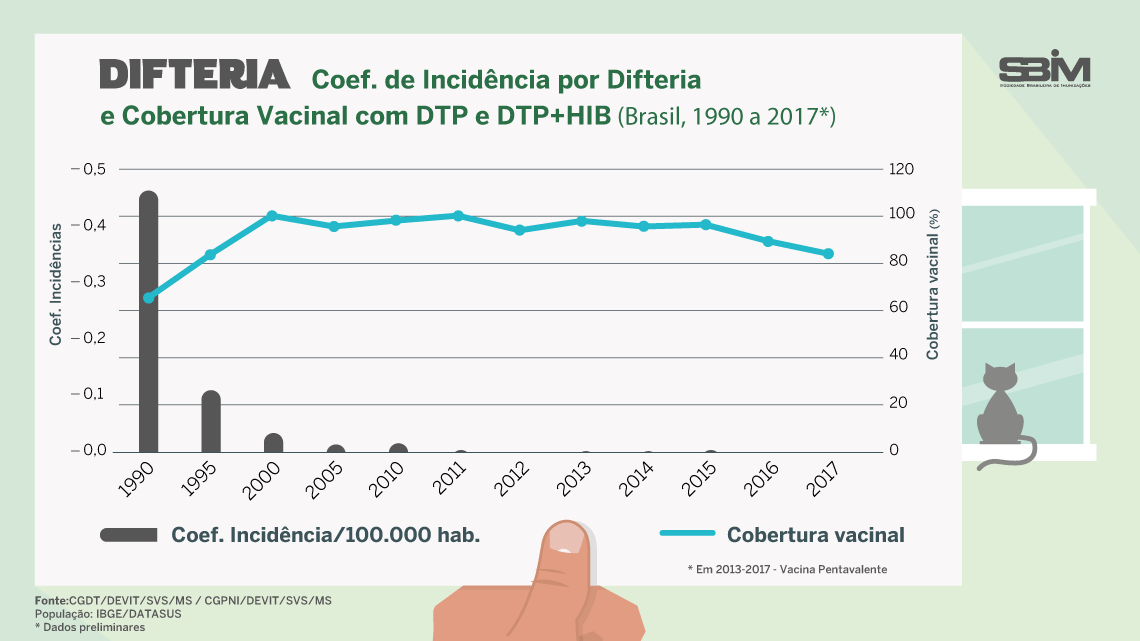
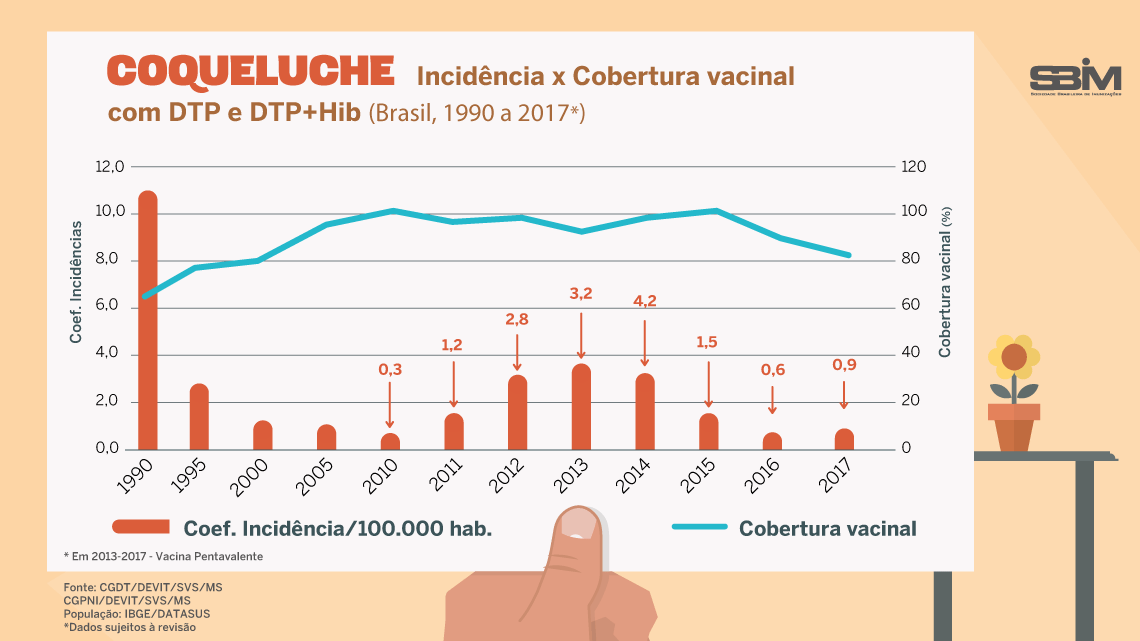
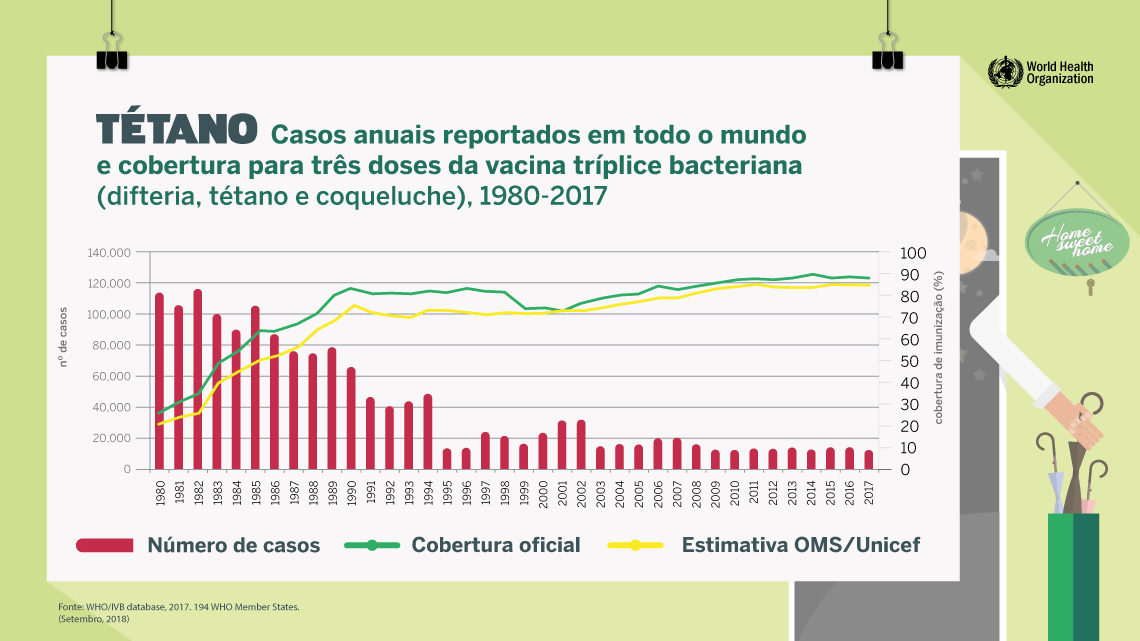
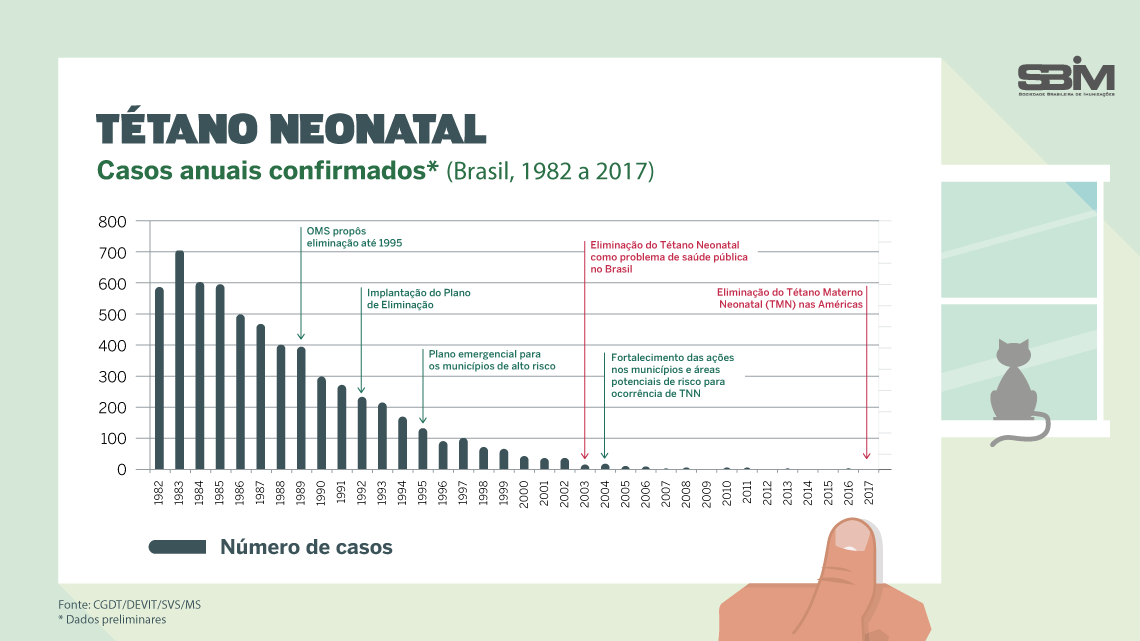
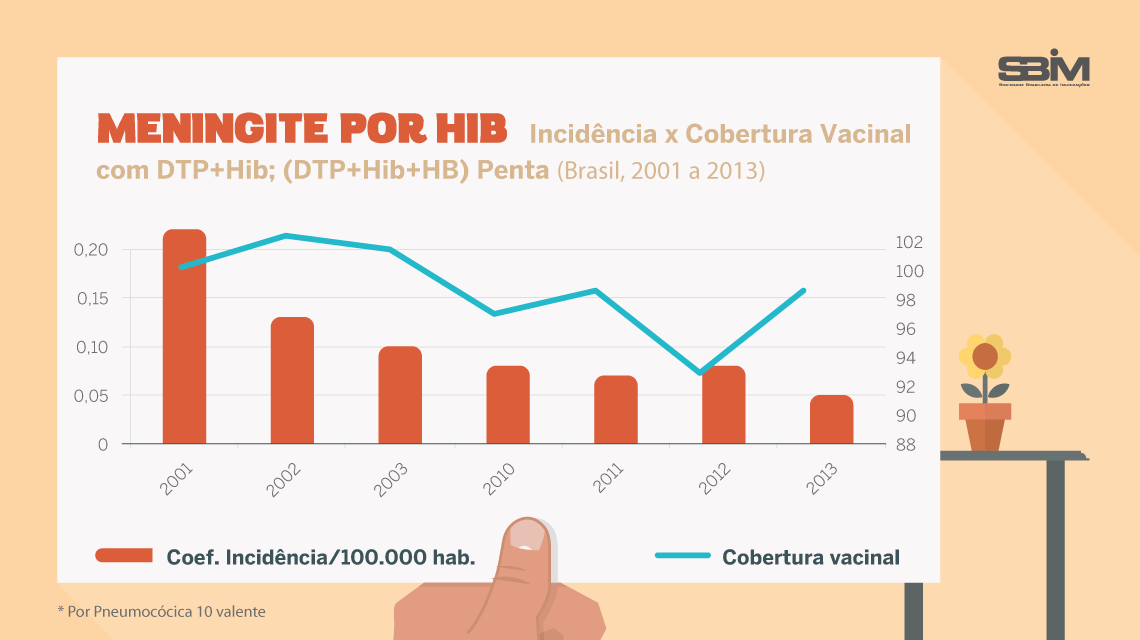
O que previne:
Difteria , tétano , coqueluche , meningite por Hib (bactéria Haemophilus influenzae tipo b) e hepatite B .
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
É composta por toxoides diftérico e tetânico, combinados com a célula inteira purificada da bactéria da coqueluche (Bordetela pertussis); partícula da superfície do vírus da hepatite B (HBsAg) e componente da cápsula do Haemophilus influenzae tipo b (Hib), conjugado com uma proteína. Contém também fosfato de alumínio, cloreto de sódio e água para injeção.
Indicação:
Crianças até 7 anos de idade.
É utilizada nas Unidades Básicas de Saúde para a vacinação no primeiro ano de vida, aos 2, 4 e 6 meses.
Mesmo as crianças que já tiveram tétano, difteria, doença causada pelo Hib e/ou coqueluche, devem ser imunizadas, uma vez que estas doenças não conferem proteção permanente contra novas infecções.
Contraindicações:
Esquema de doses:
Uma dose aos 2, 4 e 6 meses de idade.
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Pode provocar vários eventos adversos, quase sempre entre as primeiras 48 a 72 horas, sendo o componente pertussis o principal responsável. Em geral, são eventos leves, que melhoram sem complicações ou sequelas e não contraindicam doses subsequentes.
Estes eventos são os mesmos e com frequência semelhantes aos observados com a vacina tríplice bacteriana de células inteiras (DTPw).
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Do que é feita:
Tratam-se de vacinas inativadas, portanto, não têm como causar doença.
DTPa-VIP/Hib: Além dos componentes da vacina tríplice bacteriana acelular (DTPa ), contém componente da bactéria Haemophilus influenzae tipo b conjugado e vírus inativados (mortos) da poliomielite tipos 1, 2 e 3. A composição inclui ainda: lactose , cloreto de sódio, 2-fenoxietanol, hidróxido de alumínio e água para injeção. Pode conter traços de antibiótico (estreptomicina, neomicina e polimixina B), formaldeído e soroalbumina de origem bovina.
DTPa-VIP-HB/Hib: Além dos componentes da vacina tríplice bacteriana acelular (DTPa ), contém componente da bactéria Haemophilus influenzae tipo b conjugado, vírus inativados (mortos) da poliomielite tipos 1, 2 e 3 e componente da superfície do vírus da hepatite B. A composição inclui ainda: lactose, cloreto de sódio, 2-fenoxietanol, hidróxido de alumínio e água para injeção. Pode conter traços de antibiótico (estreptomicina, neomicina e polimixina B), formaldeído e soroalbumina de origem bovina.
Indicação:
As duas vacinas são recomendadas para crianças a partir de 2 meses de idade e podem ser aplicadas até os 7 anos, sempre que seja indicada cada uma das vacinas incluídas nessas combinações.
Contraindicações:
Esquema de doses:
Para a vacinação rotineira de crianças (aos 2, 4, 6 meses e entre 12 e 18 meses), preferir o uso da vacina quíntupla (penta) ou sêxtupla (hexa). Veja DTPa-VIP/Hib ou DTPa-VIP-HB/Hib . Para reforço entre 4 e 5 anos de idade, recomenda-se o uso de DTPa ou dTpa-VIP .
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Do que é feita:
No Brasil estão disponíveis duas vacinas: a produzida por Bio-Manguinhos – Fiocruz, utilizada pela rede pública, e a produzida pela Sanofi Pasteur, utilizada pelos serviços privados de vacinação e eventualmente pela rede pública. Ambas são elaboradas a partir de vírus vivo atenuado, cultivado em ovo de galinha. A vacina de Biomanguinhos apresenta em sua formulação gelatina bovina, eritromicina, canamicina, cloridrato de L-histidina, L-alanina, cloreto de sódio e água para injeção. Já a da Sanofi Pasteur contém: lactose, sorbitol, cloridrato de L-histidina, L-alanina e solução salina.
As duas têm perfis de segurança e eficácia semelhantes, estimados em mais de 95% para maiores de 2 anos.
É importante ressaltar que os estudos para o uso de doses fracionadas, recomendado apenas durante campanhas do Ministério da Saúde, em localidades e períodos bem definidos, foram realizados apenas com a vacina de Bio-Manguinhos. Não há, portanto, autorização para a administração de doses fracionadas da vacina da Sanofi Pasteur.
Indicação:
Pessoas a partir de 9 meses de idade.
Contraindicações:
Grupos com precaução para vacinação:
Em situações de aumento das chances de infecção pelo vírus selvagem da febre amarela, a vacinação pode ser recomendada para pessoas com algumas condições clínicas que inicialmente seriam consideradas contraindicação. Cabe a(o) médico(a) avaliar a relação risco-benefício.
Esquema de doses:
Rotina
Observação: O Ministério da Saúde usou em 2018 doses fracionadas como forma de conter o surto vigente na ocasião. A estratégia é reconhecida pela Organização Mundial de Saúde (OMS) como segura e eficaz
Exigência de vacinação para viajantes
Como o Brasil é considerado endêmico para a febre amarela, alguns países (acesse a lista) só permitem a entrada de viajantes brasileiros que apresentem o Certificado Internacional de Vacinação e Profilaxia (CIVP) com registro de dose aplicada no mínimo 10 dias da viagem. A dose fracionada não é válida para esse fim.
Para obter o documento é necessário procurar os serviços públicos ou privados habilitados ou acessar o site da Agência Nacional de Vigilância Sanitária (Anvisa) para emissão online. Mais informações em https://www.gov.br/pt-br/servicos/obter-o-certificado-internacional-de-vacinacao-e-profilaxia ou por meio do telefone 0800-642-9782.
Quando há contraindição para a vacinação, o médico(a) poderá emitir o certificado de isenção da vacinação contra febre amarela com a justificativa da isenção. Para informações sobre como obter este certificado, acesse https://civnet.anvisa.gov.br/app/viajante/login?wicket-crypt=CMd8D9wZbAY
Via de aplicação:
Subcutânea.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
É composta por polissacarídeos da cápsula da bactéria (Salmonella typhi), fenol, cloreto de sódio, fosfato dissódico diidratado, fosfato monossódico diidratado e água para injeção.
Indicação:
Contraindicação:
Hipersensibilidade conhecida a qualquer um dos componentes da vacina.
Esquema de doses:
Uma dose. A vacina confere proteção por três anos, de modo que a revacinação pode ser recomendada após este período, se o risco de adoecimento persistir ou retornar.
Via de aplicação:
Intramuscular ou subcutânea.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
A vacina febre tifoide causa poucas reações, sendo as mais frequentes relacionadas com o local da aplicação: dor, em 3,6% a 9,4% dos vacinados; vermelhidão, em 2,4% a 5,4%; inchaço, em 1,7% a 1,8%. Outras possíveis reações: febre, em 1,5% a 16,2%; dor de cabeça, em 10% a 7,8%; mal-estar, em 0,9% a 4%; náuseas, em 2,1% a 5%; e coceira, em 1,7% a 1,8%.
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Infecção pelo vírus Influenza (que causa a gripe ) contidos nas vacinas.
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
Sua formulação contém proteínas de diferentes cepas do vírus Influenza definidas ano a ano conforme orientação da Organização Mundial da Saúde (OMS), que realiza a vigilância nos hemisférios Norte e Sul. As cepas vacinais são cultivadas em ovos embrionados de galinha e, por isso, as vacinas contêm traços de proteínas do ovo.
Existe vacina trivalente, com duas cepas de vírus A e uma cepa de vírus B, e vacina quadrivalente, com duas cepas de vírus A e duas cepas de vírus B.
Quando a apresentação é monodose, ou seja, em seringas prontas com doses individuais, a vacina não contém conservantes. Já a apresentação multidose, como acontece com outras vacinas, contém timerosal (derivado do mercúrio ) como conservante.
Podem conter traços de formaldeído e antibióticos (geralmente gentamicina ou neomicina), utilizados durante a fabricação para prevenir contaminação por germes. Também contém cloreto de sódio e água para injeção.
Indicação:
Para todas as pessoas a partir de 6 meses de vida, principalmente aquelas de maior risco para infecções respiratórias, que podem ter complicações e a forma grave da doença.
Contraindicação:
Pessoas com alergia grave (anafilaxia), a algum componente da vacina ou a dose anterior.
Esquemas de doses:
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Sabe-se que a Síndrome de Guillain-Barré (SGB) pode ocorrer por mais de um motivo, mas em raras ocasiões seu surgimento coincidiu com a aplicação de uma vacina – nesses casos, surgiu entre um dia e seis semanas após a vacinação. Com exceção de uma vacina específica para gripe suína de 1976, todos os demais estudos que buscaram relação de causa entre vacinas influenza e SGB obtiveram resultados contraditórios, alguns encontrando essa relação e outros não. Até hoje não se sabe se a vacina influenza pode de fato aumentar o risco de recorrência da SGB em indivíduos que já a tiveram. Também é importante saber que alguns vírus podem desencadear essa síndrome.
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
É composta por antígeno do vírus da hepatite A, sal de alumínio amorfo, estabilizante (varia conforme o fabricante), cloreto de sódio a 0,9%. Pode conter traços de antibiótico (neomicina), fenoxietanol e formaldeído.
Nos serviços privados de vacinação estão disponíveis as apresentações pediátrica (para uso até 15, 17 ou 19 anos de idade, dependendo do fabricante) e de adultos.
Indicação:
Todas as pessoas a partir de 12 meses de vida.
Contraindicação:
Pessoas que tiveram reação anafilática a algum componente da vacina ou a dose anterior.
Esquema de doses:
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Infecção do fígado (hepatite) causada pelo vírus da hepatite B .
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
É composta por proteína de superfície do vírus da hepatite B purificado, hidróxido de alumínio, cloreto de sódio e água para injeção. Pode conter fosfato de sódio, fosfato de potássio e borato de sódio.
A rede pública utiliza a apresentação multidose (mais de uma dose por frasco), que contém timerosal (derivado do mercúrio) como conservante.
Indicação:
Para pessoas de todas as faixas etárias. Faz parte da rotina de vacinação das crianças, devendo ser aplicada, de preferência, nas primeiras 12-24 horas após o nascimento, para prevenir hepatite crônica – forma que acomete 90% dos bebês contaminados ao nascer.
Especialmente indicada para gestantes não vacinadas.
Contraindicação:
Não deve ser aplicada em pessoas que apresentaram anafilaxia com qualquer componente da vacina ou com dose anterior. Ou nas que desenvolveram púrpura trombocitopênica após dose anterior de vacina com componente hepatite B.
Esquema de doses:
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Infecções do fígado (hepatites) causadas pelos vírus da hepatite A e hepatite B .
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
É composta do vírus inativado (morto) da hepatite A e da proteína de superfície do vírus da hepatite B. Também possui em sua composição: sais de alumínio, formaldeído, sulfato de neomicina, fenoxietanol, polissorbato 20, cloreto de sódio e água para injeção.
Indicação:
Contraindicação:
Esquemas de doses:
Via de aplicação:
Intramuscular profunda.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Reações no local da aplicação, como vermelhidão e inchaço por mais de 24 horas e dor intensa foram relatados por 1,5% dos vacinados. Eventos gerais como febre, dor de cabeça, mal-estar, cansaço, náusea e vômito ocorrem com 0,3% a 10% dos vacinados. Não há relato de eventos adversos graves, mas podemos esperar o mesmo risco que existe para as vacinas isoladas hepatite A e hepatite B .
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
O herpes zóster , popularmente conhecido como “cobreiro”, e sua principal complicação, a neuropatia pós-herpética, responsável por dor crônica, prolongada, de difícil controle e extremamente debilitante.
Do que é feita:
Trata-se de vacina composta por vírus vivos atenuados da varicela zóster (VVZ) da cepa Oka/Merck, sacarose, gelatina, ureia, cloreto de sódio, levoglutamato de sódio monoidratado, fosfato de sódio dibásico, fosfato de potássio monobásico, cloreto de potássio, traços de neomicina e de soro de bezerro e água para injeção. Não contém conservantes.
Indicação:
A vacina está licenciada para pessoas com 50 anos ou mais e é recomendada como rotina para maiores 60 anos de idade.
Contraindicação:
Esquema de doses:
Uma dose.
Local de aplicação:
Subcutânea.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
A segurança da vacina foi avaliada em mais de 30 mil indivíduos acima de 50 anos, inclusive em maiores de 60, 70 e 80 anos, mesmo naqueles com doenças de base (cardiopatias, pneumopatias, diabetes, etc.).
A incidência de eventos adversos no local da aplicação foi de 34% nos indivíduos que receberam a vacina e de 6% nos indivíduos do estudo que receberam placebo ao invés de vacina. Em geral, foram manifestações de leves a moderadas: coceira, vermelhidão, inchaço, dor.
Entre os eventos gerais relatados estão:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Doenças causadas pelo Haemophilus influenzae tipo b, principalmente meningite .
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
É composta de pó liofilizado com polissacarídeo da cápsula da bactéria Haemophilus influenzae tipo b (Hib) conjugado com toxoide tetânico, lactose, cloreto de sódio, água para injeção. As apresentações multidose contêm fenol. Na vacina disponível na rede pública há timerosal (derivado do mercúrio).
Pode ser encontrada isolada ou combinada com a vacina tríplice bacteriana (DTPw ou DTPa ).
Indicação:
Contraindicação:
Pessoas que apresentaram anafilaxia provocada por qualquer componente da vacina ou por dose anterior.
Esquemas de doses:
Via de aplicação:
Subcutânea ou intramuscular (nunca pelas vias intravascular ou intradérmica).
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Infecções persistentes e lesões pré-cancerosas causadas pelos tipos de HPV 6,11,16,18. Também previne o câncer de colo do útero, da vulva, da vagina, do ânus e verrugas genitais (condiloma).
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
É composta pelas proteínas L1 dos papilomavírus humano (HPV) tipos 6,11,16,18, sulfato de hidroxifosfato de alumínio, cloreto de sódio, L-histidina, polissorbato 80, borato de sódio e água para injeção.
Indicação:
Contraindicação:
Gestantes e pessoas que apresentaram anafilaxia após receber uma dose da vacina ou a algum de seus componentes.
Esquemas de doses:
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Na Inglaterra, após dois anos de incorporação da vacina no calendário do governo, e da administração de 4,5 milhões de doses, somaram-se 4.703 eventos adversos. Desse total, 17% foram manifestações no local da aplicação (dor, vermelhidão e inchaço); 11%, manifestações alérgicas (urticária e prurido); e 37%, manifestações gerais como náuseas, vômitos e dor de cabeça. Foram registradas ainda reações psicogênicas (21%) descritas como pânico e desmaios causados pelo medo da injeção e não pela vacina – principalmente em adolescentes e mulheres jovens. Não ocorreu nenhum caso de doença neurológica, paralisia ou doença autoimune.
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Meningites e infecções generalizadas (doenças meningocócicas ) causadas pela bactéria meningococo do tipo B.
Do que é feita:
Trata-se de vacina inativada, portanto, não causa infecção.
É composta por quatro componentes (três proteínas subcapsulares e vesículas da membrana externa do meningococo B), além de hidróxido de alumínio, cloreto de sódio, histidina, sacarose e água para injeção.
Indicação:
Contraindicação:
Pessoas que tiveram anafilaxia após uso de algum componente da vacina ou após dose anterior.
Esquema de doses:
| Faixa etária de início da vacinação | Número de doses do esquema primário | Intervalo entre doses | Reforço |
|---|---|---|---|
| 3 a 11 meses | Duas doses | Dois meses | Uma dose entre 12 e 15 meses |
| 12 a 23 meses | Duas doses | Dois meses | Uma dose, com intervalo de 12 a 23 meses da última dose |
| A partir dos 24 meses | Duas doses | Um mês | Não foi estabelecida a necessidade de reforços |
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
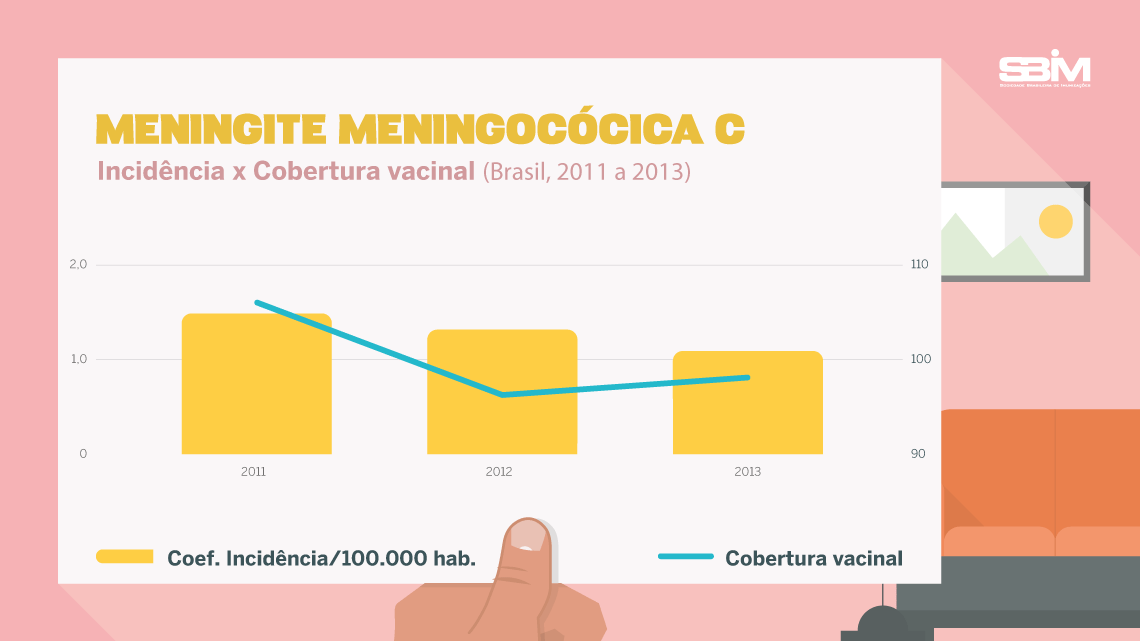
O que previne:
Doenças causadas pelo meningococo C (incluindo meningite e meningococcemia).
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença .
Contém antígeno formado por componente da cápsula da bactéria (oligossacarídeo) do sorogrupo C conjugado a uma proteína que, dependendo do fabricante, pode ser o toxoide tetânico ou o mutante atóxico da toxina diftérica, chamado CRM 197. Contém também adjuvante hidróxido de alumínio, manitol, fosfato de sódio monobásico monoidratado, fosfato de sódio dibásico heptaidratado, cloreto de sódio e água para injeção.
Indicação:
Contraindicação:
Pessoas que tiveram anafilaxia após uso de algum componente da vacina ou a dose anterior.
Esquemas de doses:
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Meningites e infecções generalizadas (doenças meningocócicas) causadas pela bactéria meningococo dos tipos A, C, W e Y.
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
Contém antígenos das cápsulas dos meningococos dos sorogrupos A, C, W e Y conjugados a uma proteína que, dependendo do fabricante, pode ser o toxoide tetânico, diftérico, ou o mutante atóxico da toxina diftérica, chamado CRM-197. Pode conter também sacarose; trometamol; fosfato de potássio diidrogenado; cloreto de sódio; fosfato de sódio diidrogenado monoidratado; fosfato dissódico hidrogenado diidratado; cloreto de sódio e água para injeção.
Indicação:
Contraindicação:
Pessoas que tiveram anafilaxia após o uso de algum componente da vacina ou após dose anterior.
Esquema de doses:
Via de aplicação:
Exclusivamente pela via intramuscular profunda.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Doenças causadas por 23 tipos de pneumococos .
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
É composta de partículas purificadas (polissacarídeos) das cápsulas de 23 tipos de Streptococos pneumoniae (pneumococo), cloreto de sódio, água para injeção e fenol.
Indicação:
Contraindicação:
Crianças, adolescentes e adultos que apresentaram anafilaxia causada por algum componente ou dose anterior da vacina.
Esquemas de doses:
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
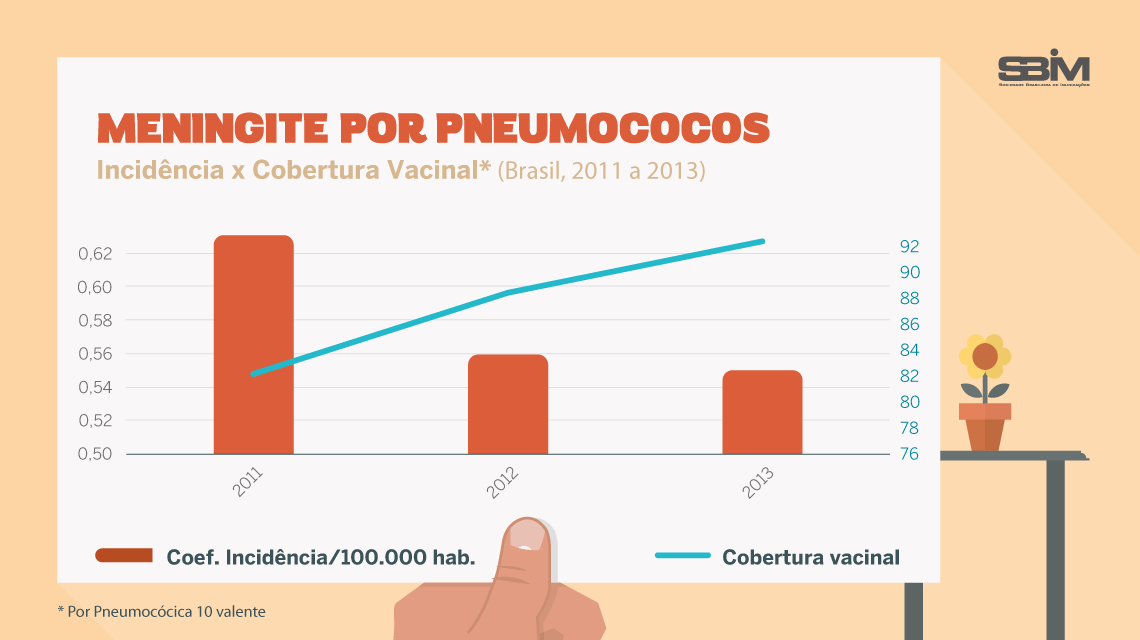
O que previnem:
A vacina pneumocócica conjugada 10-valente (VPC10) previne cerca de 70% das doenças graves (pneumonia, meningite, otite ) em crianças, causadas por dez sorotipos de pneumococos.
A vacina pneumocócica conjugada 13-valente (VPC13) previne cerca de 90% das doenças graves (pneumonia, meningite, otite ) em crianças, causadas por 13 sorotipos de pneumococos.
Do que são feitas:
Tratam-se de vacinas inativadas, portanto não têm como causar as doenças.
A VPC10 é composta de dez sorotipos de Streptococcus pneumoniae (pneumococo), oito deles conjugados com a proteína D do Haemophilus influenzae tipo b, um com o toxoide tetânico e outro com toxoide diftérico. Contém também cloreto de sódio, fosfato de alumínio e água para injeção.
A VPC13 é composta de 13 sorotipos de Streptococcus pneumoniae (pneumococo) conjugados com a proteína CRM197. Contém também sais de alumínio, cloreto de sódio, ácido succínico, polissorbato 80 e água para injeção.
Indicações:
Contraindicação:
Crianças que apresentaram anafilaxia após usar algum componente da vacina ou após dose anterior da vacina.
Esquemas de doses:
VPC10 ou VPC13
Crianças que começam a vacinação com atraso, após os 6 meses de vida, precisam que seus esquemas sejam adaptados de acordo com a idade de início. Crianças vacinadas com a VPC10 podem ser beneficiadas pela VPC13. A vacina deve ser administrada no mínimo dois meses após a última VPC10 e o númer de doses dependerá do recomendado para a idade em que a primeira dose de VPC13 for aplicada.
VPC13
Crianças menores de 6 anos que completaram o esquema de vacinação nas Unidades Básicas de Saúde com a vacina VPC10 têm benefícios se tomarem mais uma dose da VPC13, o que aumenta a proteção contra a doença pneumocócica. O número de doses dependerá da idade em que a primeira dose de VPC13 for aplicada.
Via de aplicação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Poliomielite (paralisia infantil).
Do que é feita:
Vacina Oral Poliomielite (VOP) – É uma vacina oral atenuada bivalente, ou seja, composta pelos vírus da pólio tipos 1 e 3, vivos, mas “enfraquecidos”. Contém ainda cloreto de magnésio, estreptomicina, eritromicina, polissorbato 80, L-arginina e água destilada.
Vacina Inativada Poliomielite (VIP) – Por ser inativada, não tem como causar a doença. É uma vacina trivalente e injetável, composta por partículas dos vírus da pólio tipos 1, 2 e 3. Contém ainda 2-fenoxietanol, polissorbato 80, formaldeído, meio Hanks 199, ácido clorídrico ou hidróxido de sódio. Pode conter traços de neomicina, estreptomicina e polimixina B, utilizados durante a produção.
Indicação:
Contraindicação:
Esquemas de doses:
Via de aplicação:
Cuidados antes, durante e após a vacinação:
Nota: A VOP não deve ser administrada em bebês que se encontram hospitalizados. Também não deve ser administrada em crianças que convivem com imunodeprimidos.
Efeitos e eventos adversos:
Nas apresentações combinadas com outras vacinas, os eventos adversos possíveis também se relacionam às outras vacinas que estão combinadas (ver DTPa-Hib-VIP , DTPa-Hib-VIP-HB e dTpa-VIP ).
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Raiva .
Do que é feita:
Trata-se de vacina inativada, portanto, não tem como causar a doença.
Contém vírus inativados (mortos) da raiva, maltose, albumina humana, cloreto de sódio e água para injeção. Pode conter traços de estreptomicina, neomicina e polimixina B, antibióticos usados no cultivo do vírus vacinal.
Indicação:
Contraindicação:
Esquema de doses:
Via de aplicação:
Intramuscular.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Dor, coceira e inchaço no local de aplicação e erupção de pele semelhante a urticária são relatadas em 15% a 25% dos vacinados.
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Doença diarreica causada por rotavírus .
Do que é feita:
Vacina oral monovalente (VRH1) contém um tipo de rotavírus vivo “enfraquecido”, além de sacarose, adipatodissódico, meio Eagle modificado Dulbecco (DMEM) e água estéril.
Vacina oral atenuada pentavalente (VRH5) é composta por cinco tipos de rotavírus vivos “enfraquecidos”, sacarose, citrato de sódio, fosfato de sódio monobásico monoidratado, hidróxido de sódio, polissorbato 80, meios de cultura e traços de soro fetal bovino.
Indicação:
Bebês de 6 semanas a 8 meses e 0 dia. A primeira dose deve ser obrigatoriamente aplicada até a idade de 3 meses e 15 dias, e a última dose até os 7 meses e 29 dias.
Contraindicação:
Crianças fora da faixa etária citada acima; com deficiências imunológicas por doença ou uso de medicamentos que causam imunossupressão; com alergia grave (urticária disseminada, dificuldade respiratória e choque anafilático) provocada por algum dos componentes da vacina ou por dose anterior da mesma; e com doença do aparelho gastrintestinal ou história prévia de invaginação intestinal.
Esquema de doses:
Via de aplicação:
Oral.
Cuidados antes, durante e após a vacinação:
Onde pode ser encontrada:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Do que é feita:
Trata-se de vacina atenuada, contendo vírus vivos “enfraquecidos” do sarampo, da rubéola e da caxumba; aminoácidos; albumina humana; sulfato de neomicina; sorbitol e gelatina. Contém também traços de proteína do ovo de galinha usado no processo de fabricação da vacina.
No Brasil, uma das vacinas utilizadas na rede pública contém traços de lactoalbumina (proteína do leite de vaca).
Indicação:
Crianças, adolescentes e adultos.
Contraindicação:
Esquemas de doses:
Via de aplicação:
Subcutânea.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Sarampo , caxumba , rubéola e varicela .
Do que é feita:
Trata-se de vacina atenuada, contendo vírus vivos “enfraquecidos” do sarampo, da rubéola, da caxumba e da varicela (catapora), lactose anidra, sorbitol, manitol, aminoácidos, traços de neomicina e água para injeção. Contém traços de proteína do ovo de galinha usado no processo de fabricação da vacina.
Indicação:
Contraindicação:
Esquemas de doses:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O que previne:
Do que é feita:
Trata-se de vacina atenuada, contendo vírus vivos “enfraquecidos” da varicela, além de gelatina, traços de neomicina, água para injeção. Não contém traços de proteína do ovo de galinha.
Indicação:
Contraindicação:
Esquema de doses:
Via de aplicação:
Subcutânea.
Cuidados antes, durante e após a vacinação:
Efeitos e eventos adversos:
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
O palivizumabe não é uma vacina, mas uma imunoglobulina – um tipo de anticorpo “pronto” que induz imunização passiva específica contra o vírus sincicial respiratório (VSR). Está incluído aqui porque é a única forma disponível, hoje, para a prevenção de quadros graves de infecções respiratórias em lactentes, como a bronquiolite e, principalmente, pneumonias. Até o momento não dispomos de vacinas contra o VSR.
O que previne
As formas graves de infecção pelo vírus sincicial respiratório (VSR), em bebês de alto risco.
Do que é feito
Trata-se de um anticorpo específico contra o VSR, elaborado por técnica de engenharia genética (imunização passiva).
Indicação
Está indicado no Calendário de vacinação SBIm prematuro para os recém-nascidos pré-termo com menos de 29 semanas de idade gestacional no primeiro ano de vida; para aqueles nascidos entre 29 e 32 semanas, até o sexto mês; e para portadores de doenças cardíacas e pulmonares nos dois primeiros anos de vida, independente da idade gestacional.
Contraindicação
Não há contraindicações, exceto reações alérgicas a doses anteriores do produto.
Esquema de doses
São aplicadas doses mensais de15 mg/kg de peso, por cinco meses, durante o período de maior circulação do vírus (depende da região do país).
Local de aplicação
Via intramuscular no vasto lateral da coxa.
Cuidados antes, durante e após a vacinação
Não há nenhum cuidado antes ou após a administração.
Efeitos e eventos adversos
O produto é seguro e não apresenta eventos adversos importantes além de reações locais, raras, leves e transitórias.
Fonte: SBMI, 2021.
Consulte disponibilidade e preço: vacina@santalsaude.com.br
Utilizamos cookies para oferecer melhor experiência e desempenho, além de analisar como você interage no nosso site. Não armazenamos dados pessoais nesse processo. Ao utilizar este site, você concorda com o uso destes cookies.